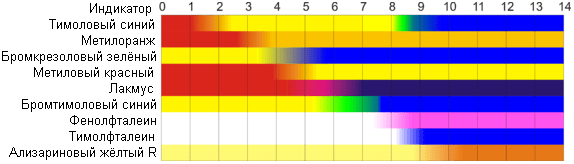
Indicatori di pH naturali
Sotto l'influenza dei cambiamenti nella reazione dell'ambiente, non solo i composti utilizzati nei laboratori come indicatori acquisiscono colori diversi. Un gruppo altrettanto numeroso è costituito dalle sostanze contenute nei prodotti naturali. In diverse prove, testeremo il comportamento degli indicatori di pH nel nostro ambiente.
Per gli esperimenti saranno necessarie diverse soluzioni con pH diverso. Possono essere ottenuti diluendo l'acido cloridrico con HCl (la soluzione di pH 3-4% è 0) e la soluzione di idrossido di sodio NaOH (la soluzione al 4% ha un pH di 14). L'acqua distillata, che useremo anche noi, ha un pH di 7 (neutro). Nello studio utilizzeremo succo di barbabietola, succo di cavolo rosso, succo di mirtillo e infuso di tè.
In provette con soluzioni preparate e acqua distillata, far cadere un po' di succo di barbabietola rossa (foto 1). In soluzioni acide acquisisce un colore rosso intenso, in soluzioni neutre e alcaline il colore diventa marrone, virando in una sfumatura gialla (foto 2). L'ultimo colore è il risultato della decomposizione del colorante in ambiente fortemente alcalino. La sostanza responsabile dello scolorimento del succo di barbabietola è la betanina. L'acidificazione dell'insalata di borscht o barbabietola è una "patatina" culinaria che conferisce al piatto un colore appetitoso.
Allo stesso modo, prova il succo di cavolo rosso (foto 3). In una soluzione acida, il succo diventa rosso vivo, in una soluzione neutra diventa viola chiaro e in una soluzione alcalina diventa verde. Anche in questo caso la base forte decompone il colorante: il liquido nella provetta diventa giallo (foto 4). Le sostanze che cambiano colore sono gli antociani. Spruzzare l'insalata di cavolo rosso con il succo di limone gli conferisce un aspetto accattivante.
Un altro esperimento richiede il succo di mirtillo (foto 5). Il colore rosso-viola vira al rosso in ambiente acido, al verde in ambiente alcalino e al giallo in ambiente fortemente alcalino (decomposizione del colorante) (foto 6). Anche qui gli antociani sono responsabili del cambiamento del colore del succo.
L'infuso di tè può essere utilizzato anche come indicatore di pH in soluzione (foto 7). In presenza di acidi il colore diventa giallo paglierino, in mezzo neutro diventa bruno chiaro, in mezzo alcalino diventa bruno scuro (foto 8). I derivati del tannino sono responsabili di cambiare il colore dell'infuso, conferendo al tè il suo caratteristico sapore aspro. L'aggiunta di succo di limone rende più chiaro il colore dell'infuso.
Vale anche la pena condurre autonomamente test con altri indicatori naturali: molti succhi e decotti di piante cambiano colore a causa dell'acidificazione o dell'alcalinizzazione dell'ambiente.
Guardalo in video:
Indicatori di pH naturali
