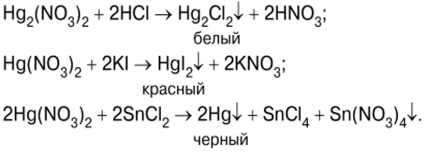
Reazioni dei composti del mercurio
Il mercurio metallico e i suoi composti sono altamente tossici per gli organismi viventi. Ciò è particolarmente vero per i composti altamente solubili in acqua. Bisogna fare molta attenzione quando si sperimentano le combinazioni di questo elemento unico (il mercurio è l'unico metallo liquido a temperatura ambiente). Rispetto dei precetti base di un chimico? ti permetterà di condurre in sicurezza diversi esperimenti con i composti del mercurio.
Nel primo esperimento otteniamo l'amalgama di alluminio (una soluzione di questo metallo in mercurio liquido). Mercurio (II) soluzione Hg nitrato (V) Hg (NO3)2 e un pezzo di filo di alluminio (foto 1). Un'asta di alluminio (pulita accuratamente dai depositi) viene posta in una provetta con una soluzione di un sale di mercurio solubile (foto 2). Dopo qualche tempo, possiamo osservare il rilascio di bolle di gas dalla superficie del filo (foto 3 e 4). Dopo aver rimosso l'asta dalla soluzione, si scopre che l'argilla è ricoperta da un rivestimento soffice e, inoltre, vediamo anche palline di mercurio metallico (foto 5 e 6).
Chimica: l'esperienza di combinare il mercurio
In condizioni normali, la superficie dell'alluminio è ricoperta da uno strato aderente di ossido di alluminio.2O3isola efficacemente il metallo dalle influenze ambientali aggressive. Dopo aver pulito e immerso l'asta in una soluzione di sale di mercurio, gli ioni Hg vengono spostati2+ alluminio più attivo
Il mercurio depositato sulla superficie dell'asta forma un amalgama con l'alluminio, il che rende difficile l'adesione dell'ossido. L'alluminio è un metallo molto attivo (reagisce con l'acqua per rilasciare idrogeno - si osservano bolle di gas) e il suo utilizzo come materiale strutturale è possibile grazie al denso rivestimento di ossido.
Nel secondo esperimento rileveremo ioni NH di ammonio.4+ utilizzando il reagente di Nessler (il chimico tedesco Julius Nessler fu il primo ad usarlo in analisi nel 1856).
Esperimento sulla reazione del luppolo e dei composti del mercurio
Il test inizia con la precipitazione dello ioduro di mercurio (II) HgI.2, dopo aver miscelato soluzioni di ioduro di potassio KI e nitrato di mercurio (II) (V) Hg (NO3)2 (foto 7):
Precipitato rosso arancio di HgI2 (foto 8) quindi trattato con un eccesso di soluzione di ioduro di potassio per ottenere un composto complesso solubile di formula K2HgI4 ? Potassio tetraiodercurato (II) (Foto 9), che è il reagente di Nessler:
Con il composto risultante, possiamo rilevare gli ioni di ammonio. Saranno comunque necessarie soluzioni di idrossido di sodio NaOH e cloruro di ammonio NH.4Cl (foto 10). Dopo aver aggiunto una piccola quantità di soluzione di sale di ammonio al reagente Nessler e aver alcalinizzato il mezzo con una base forte, si osserva la formazione di un colore giallo-arancione del contenuto della provetta. La reazione attuale può essere scritta come:
Il composto di mercurio risultante ha una struttura complessa:
Il test di Nessler ad alta sensibilità viene utilizzato per rilevare anche tracce di sali di ammonio o ammoniaca nell'acqua (ad es. acqua del rubinetto).

